-
铬 编辑
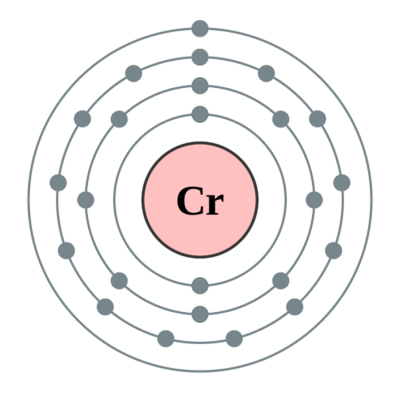
铬(Chromium),化学符号Cr,原子序数为24,在元素周期表中属ⅥB族。元素名来自于希腊文,原意为“颜色”,因为铬的化合物都有颜色。单质为钢灰色金属,是自然界硬度最大的金属。铬在地壳中的含量为0.01%,居第17位。呈游离态的自然铬极其罕见,主要存在于铬铅矿中。相对密度7.15g/cm³,熔点1907℃,沸点2679℃。电阻率12.7x10⁻⁸Ω·m(20℃)。铬是一种蓝灰色、非常耀眼光泽的坚硬金属。铬的化合物都有毒,地球上的铬以铬铁矿的形式存在。铬主要用于不锈钢、电镀和金属陶瓷等。微量铬是生命的必需元素,铬的中毒量为200mg,致死量大于3g。高价铬有致癌作用。
中文名:铬
外文名:chromium
化学式:Cr
分子量:52.01
CAS登录号:7440-47-3
EINECS登录号:231-157-5
熔点:1907 ℃
沸点:2679 ℃
密度:7.15 g/cm³(固体)
外观:钢灰色金属
安全性描述:S16;S26;S27;S36/37/39;S45
危险性符号:Xn
危险性描述:R40
UN危险货物编号:2924
 克拉普罗特
克拉普罗特
1797年,沃克兰发现了氧化铬。
1798年,沃克兰给他找到的这种灰色针状金属命名为chrom,来自希腊文chroma(颜色)。由此得到铬的拉丁名称chromium和元素符号Cr。差不多在同一个时期里,克拉普罗特也从铬铅矿中独立发现了铬。
2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,金属铬在3类致癌物清单中。
物理性质
 金属铬块,玻封铬展示标本
金属铬块,玻封铬展示标本
铬具有很高的耐腐蚀性,在空气中,即便是在赤热的状态下,氧化也很慢。不溶于水。镀在金属上可起保护作用。
化学性质
铬与卤素单质的反应
在400℃和200—300atm下,铬直接同氟气反应生成氟化铬(Ⅵ)CrF₆。
在比较温和的条件下,可以生成氟化铬(Ⅴ)CrF₅。%20
在更温和的条件下,铬同氟气(F₂)、氯气(Cl₂)、溴单质(Br₂)、碘单质(I₂)分别反应生成相应的三卤化物氟化铬(Ⅲ)(CrF₃)、氯化铬(Ⅲ)(CrCl₃)、溴化铬(Ⅲ)(CrBr₃)和碘化铬(Ⅲ)(CrI₃)。%20
铬与酸的反应
金属铬能迅速溶解在稀盐酸中,形成氢气和包含铬(Ⅱ)离子的水溶液。实际上Cr(Ⅱ)是以Cr(H₂O)₆²⁺配离子的形式存在的。在硫酸中也有相似的情况,但是纯净的铬不会与酸发生反应,如铬不会与硝酸(HNO₃)发生反应。事实上,铬会在硝酸中纯化。%20
工业制备
实验室制备
另外一种生产铬的方法则是电解,首先需要把Cr₂O₃溶解在硫酸中,随后用所得的电解液电镀即可。%20
铬可用于制不锈钢。红、绿宝石的色彩也来自于铬。作为现代科技中最重要的金属,以不同百分比熔合的铬镍钢千变万化,种类繁多,令人难以置信。
铬的毒性与其存在的价态有关,六价铬比三价铬毒性高100倍,并易被人体吸收且在体内蓄积,三价铬和六价铬可以相互转化。天然水不含铬;海水中铬的平均浓度为0.05μg/L;饮用水中更低。铬的污染源有含铬矿石的加工、金属表面处理、皮革鞣制、印染等排放的污水。
由于铬合金性脆,作为金属材料使用还在研究中,铬主要以铁合金(如铬铁)形式用于生产不锈钢及各种合金钢。金属铬用作铝合金、钴合金、钛合金及高温合金、电阻发热合金等的添加剂。氧化铬用作耐光、耐热的涂料,也可用作磨料,玻璃、陶瓷的着色剂,化学合成的催化剂。碱式硫酸铬(三价铬盐)用作皮革的鞣剂。铬矾、重铬酸盐用作织物染色的媒染剂、浸渍剂及各种颜料。镀铬和渗铬可使钢铁和铜、铝等金属形成抗腐蚀的表层,并且光亮美观,大量用于家具、汽车、建筑等工业。此外,铬矿石还大量用于制作耐火材料。
在航空和其他产业中,可用于阳极氧化铝。
耐火材料生产中,把铬铁矿用于制砖和成型。
 铬矿石
铬矿石
截至2021年底,全球铬铁矿储量20.42亿吨。
中国铬矿资源紧缺,探明储量1309.5万吨,保有储量1095.1万吨,主要分布于西藏、新疆等地。铬铁矿有56处产地,主要是新疆萨尔托海、西藏罗布莎、内蒙古贺根山、甘肃大道尔吉等铬矿。
环境危害
三价铬对人体几乎不产生有害作用,未见引起工业中毒的报道。进入人体的铬被积存在人体组织中,代谢和被清除的速度缓慢。铬进入血液后,主要与血浆中的球蛋白、白蛋白、r-球蛋白结合。六价铬还可透过红细胞膜,15分钟内可以有50%的六价铬进入细胞,进入红细胞后与血红蛋白结合。铬的代谢物主要从肾排出,少量经粪便排出。六价铬对人主要是慢性毒害,它可以通过消化道、呼吸道、皮肤和粘膜侵入人体,在体内主要积聚在肝、肾和内分泌腺中。通过呼吸道进入的则易积存在肺部。六价铬有强氧化作用,所以慢性中毒往往以局部损害开始逐渐发展到不可救药。经呼吸道侵入人体时,开始侵害上呼吸道,引起鼻炎、咽炎和喉炎、支气管炎。
健康危害
对人皮肤
铬化合物并不损伤完整的皮肤,但当皮肤擦伤而接触铬化合物时即可发生伤害作用。铬性皮肤溃疡的发病率偶然性较高,主要与接触时间长短,皮肤的过敏性及个人卫生习惯有关。铬疮主要发生于手、臂及足部,但只要皮肤发生破损,不管任何部位,均可发生。指甲根部是暴露处,容易积留脏物,皮肤也最易破损,因此这些部位也易形成铬疮。形成铬疮前,皮肤最初出现红肿,具搔痒感,不作适当治疗可侵入深部。溃疡上盖有分泌物的硬痂,四周部隆起,中央深而充满腐肉,边缘明显,呈灰红色,局部疼痛,溃疡部呈倒锥形,溃疡面较小,一般不超过3mm,有时也可大至12—30mm,或小至针尖般大小,若忽视治疗,进一步发展可深放至骨部,剧烈疼痛,愈合甚慢。
接触六价铬也可发生铬性皮炎及湿疹,患处皮肤搔痒并形成水泡,皮肤过敏者接触铬污染物数天后即可发生皮炎,铬过敏期长达3-6月,湿疹常发生于手及前臂等暴露部份,偶尔也发生在足及踝部,甚至脸部、背部等。
对呼吸道
接触铬盐常见的呼吸道职业病是铬性鼻炎,该病早期症状为鼻粘膜充血,肿胀、鼻腔干燥、搔痒、出血,嗅觉减退,粘液分泌增多,常打喷嚏等,继而发生鼻中隔溃疹,溃疹部位一般在鼻中隔软骨前下端1.5cm处,无明显疼痛感。铬性鼻炎根据溃疡及穿孔程度,可为三期:
糜烂性鼻炎,鼻中隔粘膜縻烂,呈灰白色斑点。
溃疡性鼻炎,鼻中隔变薄,鼻粘膜呈凹性缺损,表面有浓性痂盖,鼻中粘膜苍白,嗅觉明显衰退。
鼻中隔穿孔,鼻中隔软骨可见圆形成三角形孔洞穿孔处有黄色痂,鼻粘膜萎缩,鼻腔干燥。
对眼及耳
眼皮及角膜接触铬化合物可能引起刺激及溃疡,症状为眼球结膜充血、有异物感、流泪刺痛、视力减弱,严重时可导致角膜上皮脱落。
铬化合物侵蚀鼓膜及外耳引起溃疡仅偶然发生。
对肠胃道
误食入六价铬化合物可引起口腔粘膜增厚,水肿形成黄色痂皮,反胃呕吐,有时带血,剧烈腹痛,肝肿大,严重时使循环衰竭,失去知觉,甚至死亡。六价铬化合物在吸入时是有致癌性的,会造成肺癌。
全身中毒
此种情况甚少,症状是:头痛消瘦,肠胃失调,肝功能衰竭,肾脏损伤,单接血球增多,血钙增多及血磷增多等。
毒理资料
所有铬化合物都是剧毒物。铬(Ⅵ)化合物有剧毒,并强烈致癌,铬(Ⅲ)化合物毒性较低。铬化合物是重要的污染物。
储存方法
储存于阴凉、通风的库房。远离火种、热源。应与氧化剂、酸类分开存放,切忌混储。配备相应品种和数量的消防器材。储区应备有合适的材料收容泄漏物。
运输方法
运铬铁的设备必须要有顶盖,来避免在运输的过程中,出现暴风雨的天气。
铬铁在装车之前,要先检测运输地车辆能不能够安全地运转,再就是检查车厢有没有漏洞,看一看运输地设备是否有防雨措施,检测货物地包装是否完整,是否将所有货物归类整理,然后再有顺序地放到运输设备里面。
铬铁装满车厢以后,一定要办理交接手续,确认以后再发车。
在运输的过程中,司机应该是定期检查车辆,检查顶棚,检查货物在车厢内的堆放情况,一般事故的隐患都是从泄漏开的,由于在行车的途中车辆颠簸震动,往往是会造成包装破损。
高碳铬铁厂家提醒虽然铬铁不是危险物品,但是在运输的时候,还要需要注意路线,不能为了路近选择走一些比较复杂难走的路段,同时也千万不能在城市街道和人口密集的的方停车,另外在铬铁在运输的过程中,是不可以与坚硬物质混装,也不可以强烈的振动、摩擦、踩、砸,禁止抛掷。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。