-
碳负离子 编辑
碳负离子(Carbon anion)是三个基团,有一对孤对电子的碳的活性中间体,一个单位负电荷。四面体构型。孤对电子占一个杂化轨道。比较相应酸的酸性大小,判断负离子稳定性大小。
中文名:碳负离子
外文名:Carbon anion
碳负离子是带负电荷的具有偶数价电子的粒子,其负电荷(未共用电子对)定域在一个碳原子上。甲基负离子可看作是一切碳负离子的母体,各碳负离子可以烷基负离子来命名。
由吸电子基共轭稳定化(-R效应)的碳负离子,由于实际的共振结构中负电荷主要分布在氧原子上,这类离子叫做碳负离子的性质。
一般碳负离子
碳负离子带有负电荷,中心碳原子为三价,价电子层充满八个电子,具有一对未共用电子。中心碳原子的可能构型有两种:一种为杂化的平面构型,另一种杂化的棱锥构型。
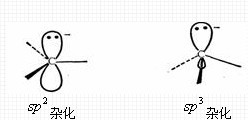 图1
图1
特殊的碳负离子
虽然环丙基正离子由于环张力不利于平面构型而很不稳定,但环丙基负离子确是存在的,因为棱锥构型对碳负离子是相对有利的。在桥环化合物中,桥头碳正离子是很不稳定的,因为环的几何形状的限制,不利于平面构型的存在,所以很少有桥头碳正离子生成。但对桥头碳负离子说,棱锥构型则是相对有利的,所以桥头碳负离子是稳定的,可以存在的。正因如此,桥头有机锂化合物容易生成,例如下面通过桥头碳负离子进行的反应是很顺利的。这也为碳负离子的棱锥构型提供了进一步的证据。但当带负电荷的中心碳原子与键或芳环相连时,由于未共用的电子对能与键发生共轭离域而稳定,这时碳负离子将取杂化的平面构型,以达到轨道最大的交盖,更好地离域,使体系能量最低最稳定。
杂化效应
杂化轨道电负性大小顺序是
根据反应式:
芳香性
具有芳香性的物质在结构上具备:是闭合的共轭体系;参加共轭的原子在一个平面上;参与共轭的p电子数符合如4n+2规则。同样,具备上述三条件的环状共轭碳负离子也具有芳香性,很稳定。
共轭效应
当碳负离子与碳碳双键或苯环直接相连时,由于共轭作用可使负电荷得到分散。因此碳负离子上连接的双键(或苯环)越多,碳负离子越稳定。共轭效应不仅使碳负离子的稳定性增加,而且使碳负离子构型也发生变化:一般碳负离子的构型为角锥型,而有共轭效应的碳负离子可为平面构型。另外碳—氮、碳—氧、氮—氧重键对碳负离子也同样有稳定作用。由于氮、氧比碳原子有较大的电负性,能更好分散负电荷,所以更能使碳负离子稳定,其碳—质酸酸性更大。
溶剂效应
一般来说,极性的质子溶剂能够使正、负离子溶剂化,而极性非质子溶剂如二甲基亚砜不能够使负离子溶剂化,因此溶剂不同,碳负离子的活性和稳定性是不同的。
有机金属化合物,如Grignard试剂和有机锂试剂也可看作是碳负离子源。叶立德,如磷叶立德和硫叶立德等,都含有具有碳负离子结构的共振杂化体。
碳负离子可进行SN2反应。
碳负离子在有机合成中有着极其重要的地位。它参与了许多重要的有机合成反应,比如:酯缩合,羟醛缩合,witting反应,麦克尔加成等。认识碳负离子有助于我们认识正确的有机合成本质。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。