-
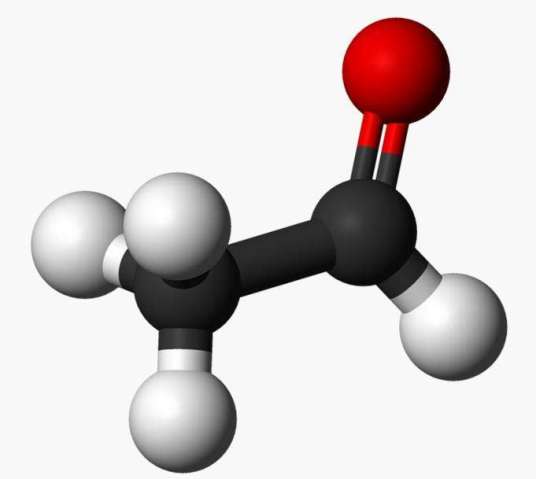
羰基化合物 编辑
有机化学中,羰基化合物指的是一类含有羰基的化合物。根据环境的不同,羰基化合物可以指:醛、酮、羧酸及羧酸衍生物(包括酸酐、酰卤、酰胺、酯等)的合称。配位化学中,羰基化合物指一类含有一氧化碳作为配体的化合物。无机化学中,羰基化合物可以指一类含有C=O键的化合物。如二氧化碳、硫化羰等。
中文名:羰基化合物
外文名:carbonyl compound
所属学科:有机化学
化学性质:亲核加成、α-活泼氢、氧化还原
物理性质:沸点比相应相对分子质量的烷烃高
包括:醛、酮、羧酸及羧酸衍生物
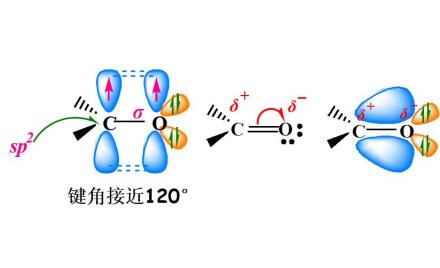 羰基
羰基
醛分子中,羰基至少要与一个氢原子直接相连,故醛基一定位于链端。
羰基化合物的命名
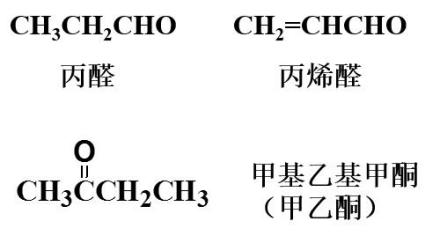
羰基化合物的命名
(1)普通命名法醛按氧化后生成的羧酸命名,酮看作是甲酮的衍生物。可用α、β、γ、δ等标记取代基位置。
(2)系统命名法
当分子中含有多种官能团时,首先要确定一个主官能团,然后,选含有主官能团及尽可能含较多官能团的最长碳链为主链。主链编号的原则是要让主官能团的位次尽可能小。命名时,根据主官能团确定母体的名称,其它官能团作为取代基用词头表示,分子中如涉及立体结构要在名称最前面表明其构型,然后根据名称的基本格式写出名称。
(2)水溶性:醛酮的氧原子可以与水形成氢键,因此低级醛酮能与水混溶。
(1)反应机理
反应过程中,一般是亲核试剂中带负电荷的部分(即亲核部分)先进攻底物中不饱和化学键带部分正电荷一端原子,并与之成键,π键断开形成另一端原子的负离子中间体,然后试剂中的亲电部分与负离子中间体结合,形成亲核加成产物。
最有代表性的反应是醛或酮的羰基与格氏试剂加成的反应:RC=O + R'MgCl → RR'C-OMgCl,再水解得醇,这是合成醇的良好办法。在羰基中,O稍显电负性;在格氏试剂中,C-Mg相连,Mg稍显电正性,C是亲核部位。于是格式试剂的亲核碳进攻亲电的羰基碳,双键打开,新的C-C键形成。
羰基可与碳为中心原子的亲核试剂加成,如格氏试剂、HCN、炔化钠。
羰基还可与氮为中心原子的亲核试剂的加成,如氨及其衍生物。
羰基还与氧为中心原子的亲核试剂的加成,如H2O、ROH等。
(2)反应应用——增长碳链
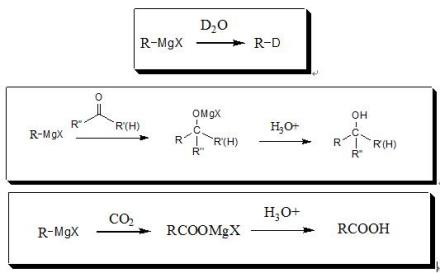 利用亲核加成反应增长碳链
利用亲核加成反应增长碳链
格氏试剂可以合成氘代烃;格氏试剂与醛、酮、酯、环氧烷发生亲核加成反应成相应的醇;反应若生成二级醇,还可以氧化成酮,再继续与格氏试剂反应生成三级醇。格氏试剂与二氧化碳作用可制备多一个碳的羧酸。
α-活泼氢引起的反应
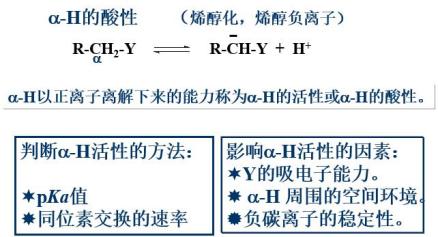 α-活泼氢引起的反应
α-活泼氢引起的反应
含有α-H的醛的存在下,在稀碱的存在下,可以互相结合生成β-羟醛基,受热后进而生成α、β-不饱和醛(有第二个α-H),通过羟醛缩合,在分子中形成了新的碳碳键,增长了碳链。
酮式、烯醇式的互变异构、醛酮的α-H卤代、卤仿反应、羟醛缩合反应等。
氧化和还原反应
(1)氧化反应
醛极易氧化,许多氧化剂都能将醛氧化成酸。脂肪醛比芳醛容易氧化。然而,将醛暴露在空气中,则是芳醛比脂肪醛容易氧化,这是因为用化学氧化剂氧化为离子型氧化反应。
酮遇一般氧化剂,抗拒氧化。酮遇强烈氧化剂,碳链断裂,形成酸。酮氧化时碳碳键断裂,一般地生成混合物,意义不大,但是环酮氧化后可得单一化合物,在制备上有意义。
酮能发生一个特殊的氧化反应:拜耳-魏立格(Baeyer-Villiger)氧化,即酮类化合物被过酸氧化,与羰基直接相连的碳链断裂,插入一个氧形成酯的反应。
(2)还原反应
 醛或酮还原成醇
醛或酮还原成醇
其他反应
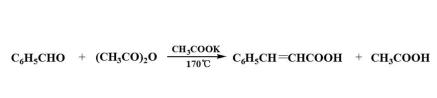 Perkin反应
Perkin反应
芳醛与含α-H的脂肪族酸酐,在相应的羧酸盐存在下共热,发生缩合生成α,β-不饱和酸,该反应称为珀金(Perkin)反应。
(2)Mannich反应
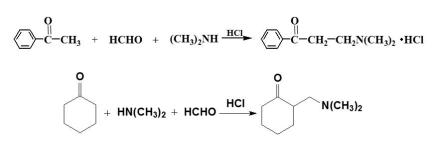 Mannich反应
Mannich反应
该反应的净结果是二甲氨甲基取代了α-H,故又称为氨甲基化反应,产物为β-氨基酮。
Mannich反应通常是在酸性溶液中进行,除醛、酮外,其它含α-H的化合物如酯、腈等也可发生该反应。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。